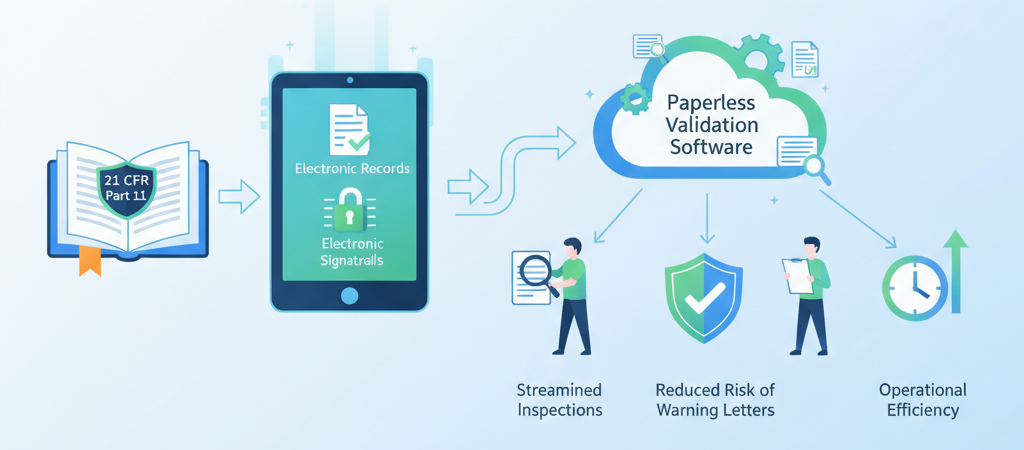
Assurer la Conformité au 21 CFR Part 11 avec des Dossiers Électroniques, des Signatures Électroniques et des Pistes d'Audit
Dans le paysage réglementé de l'industrie pharmaceutique et des sciences de la vie, le 21 CFR Part 11 de la FDA américaine établit des normes rigoureuses pour les dossiers électroniques et les signatures électroniques. Satisfaire ces exigences permet non seulement d'éviter les lettres d'avertissement, mais établit également une culture prête pour les audits qui renforce l'intégrité des données, la transparence et l'efficacité opérationnelle.
Pourquoi les Dossiers Électroniques et les Signatures Électroniques Sont Importants
Intégrité et Authenticité des Données Les dossiers électroniques, lorsqu'ils sont correctement gérés, sont inviolables et horodatés. Chaque modification est enregistrée, garantissant que les données présentées lors d'une inspection FDA sont fiables et non altérées.
Responsabilité grâce aux Signatures Électroniques La Part 11 exige que les signatures électroniques soient uniquement liées à leurs signataires et que leur identité puisse être vérifiée. Cela garantit que chaque approbation ou document est traçable à un individu spécifique, renforçant la responsabilité personnelle.
Pistes d'Audit Complètes Les pistes d'audit enregistrent automatiquement qui a fait quoi et quand — y compris la création de dossiers, les modifications, les révisions et les validations. Lors d'un audit FDA, cet historique détaillé démontre la conformité continue et décourage les modifications non autorisées.
Principaux Avantages pour des Opérations Prêtes pour les Audits
Inspections Rationalisées Avec des dossiers électroniques complets et des journaux d'audit, les inspecteurs peuvent immédiatement vérifier la conformité ; plus besoin de chercher des fichiers papier ou de reconstituer des signatures manquantes.
Risque Réduit de Lettres d'Avertissement Une documentation approfondie des contrôles de conformité — signatures électroniques, authentification des utilisateurs, contrôle d'accès basé sur les rôles — minimise le risque de citations FDA pour une tenue de dossiers inadéquate.
Efficacité Opérationnelle La transition du papier aux dossiers numériques réduit les erreurs de manipulation manuelle, accélère les cycles d'approbation et libère le personnel des tâches fastidieuses d'archivage.
Fonctionnalités Essentielles d'une Solution Logicielle Conforme à la Part 11
Validation Sans Papier Éliminez les piles de classeurs et formulaires papier. Une bibliothèque de validation numérique stocke toute la documentation — URS, protocoles de test, rapports récapitulatifs — dans un référentiel sécurisé accessible partout.
Documents de Validation Basés sur des Modèles Des modèles prêts à l'emploi pour les protocoles, les rapports de déviation et les matrices de traçabilité assurent la cohérence et le respect des directives GxP tout en réduisant considérablement le temps de préparation des documents.
Flux de Travail Configurables Définissez des pipelines électroniques de « tâches à faire » pour la révision des brouillons, les approbations des parties prenantes et la validation finale. Les notifications automatisées maintiennent les projets de validation dans les délais et visibles pour tous les membres de l'équipe.
Contrôles d'Accès Centrés sur l'Utilisateur Appliquez des autorisations strictes basées sur les rôles afin que seul le personnel autorisé puisse consulter, modifier ou valider des dossiers de validation spécifiques.
Comment GoVal Permet la Conformité au 21 CFR Part 11
Le Système de Gestion du Cycle de Vie de Validation de GoVal est conçu pour satisfaire chaque aspect de la Part 11 :
Dossiers Électroniques Sécurisés Tous les dossiers sont chiffrés au repos et en transit. Des pistes d'audit immuables capturent chaque action de l'utilisateur, complètes avec horodatages et adresses IP.
Signatures Électroniques Robustes GoVal lie chaque signature à des comptes utilisateurs authentifiés à plusieurs facteurs. Les validations ajoutent automatiquement les informations d'identification du signataire et sa justification.
Tableaux de Bord Prêts pour les Audits Une vue d'ensemble consolidée affiche le statut de conformité, les tâches ouvertes et les journaux d'audit en temps réel — éliminant les surprises et garantissant que les inspecteurs voient un système bien organisé.
Bibliothèque de Validation Sans Papier Stockez et récupérez instantanément les livrables de validation. L'archivage numérique signifie aucun fichier perdu et une récupération instantanée pour les audits ou les revues de direction.
Documents Basés sur des Modèles Des modèles prêts à l'emploi couvrent les URS, IQ/OQ/PQ, protocoles de test, rapports de déviation et rapports récapitulatifs. La personnalisation permet l'alignement avec les SOPs internes.
Flux de Travail Automatisés Configurez des flux de travail ramifiés pour acheminer les documents pour révision, approbation et signature. Les rappels automatisés et les règles d'escalade assurent l'achèvement dans les délais.
Rapports et Analyses Générez des métriques de conformité, des analyses de tendances et des résumés exécutifs en quelques clics — fournissant des informations exploitables et une transparence pour la direction et les régulateurs.
Conclusion
L'adoption d'une plateforme de validation numérique conforme à la Part 11 transforme l'approche de votre organisation en matière de conformité réglementaire. Les dossiers électroniques, les signatures et les pistes d'audit créent une chaîne de confiance ininterrompue dans vos données — réduisant considérablement les risques de lettres d'avertissement FDA et élevant votre niveau de préparation aux audits. Avec la solution sans papier, basée sur des modèles et pilotée par des flux de travail de GoVal, atteindre et maintenir la conformité au 21 CFR Part 11 devient un processus rationalisé, transparent et efficace.